Abstrato
A ausência de avanços claros no combate à malária poderia apoiar a necessidade de diferentes formas de combater a doença, fundamentadas em bases conceptualmente novas. A ideia principal desta pesquisa é analisar a possibilidade de interferir na atividade do parasita da malária utilizando frequências eletromagnéticas ressonantes específicas. Embora a ideia de combater a infecção pela malária com frequências eletromagnéticas não seja nova, apresentaremos aqui uma abordagem única, o chamado Modelo de Reconhecimento Ressonante (RRM) para identificar especificamente as frequências eletromagnéticas mais importantes para a interferência com a infecção pela malária.
O RRM calcula periodicidades (frequências) na distribuição das energias dos elétrons livres ao longo da sequência da proteína que são relevantes para a função/interação da proteína. Quando a transferência de carga através da estrutura da proteína é considerada, ela pode produzir radiação eletromagnética de frequência específica dependendo da velocidade de carga. Foram analisados dez grupos de proteínas relevantes para as interações do Plasmodium .
Cada um dos dez grupos de proteínas tem pelo menos um pico de frequência característico significativo em uma das seguintes frequências RRM: f = 0,002, f = 0,11 ou f = 0,34. Isto sugere que a diversidade de proteínas participantes na invasão do Plasmodium poderia ser representada com apenas três frequências RRM. Dependendo do mecanismo de transferência de carga (velocidade) ao longo da proteína, são esperadas diferentes frequências de ressonância eletromagnética. Com base nos resultados apresentados, sugerimos que a frequência RRM de f = 0,002 (relacionada a 2-5THz), seja considerada crucial para a infectividade do Plasmodium e possivelmente por interferir no processo de invasão. Embora esta frequência eletromagnética do infravermelho distante não possa penetrar no corpo humano mais do que 4 cm, tal radiação pode ser de grande ajuda no combate ao Plasmodium , uma vez que uma parte considerável do parasita permanece na pele durante horas após a picada do mosquito. Além disso, a frequência RRM específica é capaz de iniciar de forma ressonante toda uma cascata de interações proteína-proteína (DNA, RNA) direcionadas à atividade biológica específica que poderia contrariar a infecção por Plasmodium .
Fundo
Esta investigação é dedicada ao estudo da malária, uma das preocupações de saúde globais mais desafiadoras do nosso tempo. Nos humanos, a malária é causada por diversas espécies do parasita Plasmodium ( Plasmodium falciparum, Plasmodium vivax, Plasmodium malariae, Plasmodium ovale, Plasmodium knowlesi ). Durante seu ciclo de vida, o Plasmodium parasita o hospedeiro humano ou o mosquito Anopheles . Para isso, utiliza-se um conjunto sofisticado de mecanismos de invasão redundantes, embora o enigma desses mecanismos ainda esteja longe de ser resolvido. No nível proteômico, existem proteínas do Plasmodium interagindo com proteínas do hospedeiro humano, bem como proteínas do Plasmodium interagindo com as proteínas do mosquito Anopheles [ 1–7 ].
A ideia principal desta pesquisa é analisar a possibilidade de interferir na atividade do parasita da malária utilizando frequências eletromagnéticas ressonantes específicas. Reconhecimento ressonante em um processo não linear. A ideia de combater a infecção da malária com frequências eletromagnéticas não é nova, pois tem havido uma tentativa de projetar um sistema que possa matar mosquitos usando radiação eletromagnética infravermelha [ 8 ]. Aqui, apresentamos uma abordagem para interferir especificamente na infecção, em vez de matar mosquitos, com frequências eletromagnéticas características específicas calculadas usando uma abordagem única, não convencional e inovadora, o chamado Modelo de Reconhecimento Ressonante (RRM). O RRM propõe que as interações proteína-proteína, proteína-DNA e proteína-RNA sejam baseadas no reconhecimento ressonante eletromagnético com frequência característica distinta para cada interação [ 9–11 ] .
A abordagem RRM é baseada na descrição físico-matemática que encontrou apoio crescente ao longo dos últimos 30 anos [ 12–16 ] . De acordo com o RRM, propomos que o reconhecimento de proteínas durante a invasão do parasita ocorra através da troca de radiação eletromagnética em frequências muito específicas. Utilizamos esta abordagem única para identificar as frequências específicas de interação entre Plasmodium e células humanas e de mosquitos Anopheles , com possibilidade de interferir nessas frequências na prevenção da infecção por malária. Uma abordagem semelhante usando o RRM foi proposta para combater a infecção por Ebola [ 15 ].
Em nossa pesquisa anterior, analisamos a interação entre proteínas de Plasmodium e proteínas humanas envolvidas na infecção por malária com o objetivo de propor uma vacina candidata promissora baseada em RRM [ 17 ]. Aqui nos baseamos nesses resultados para descobrir as principais frequências específicas de reconhecimento inicial entre Plasmodium e proteínas humanas, bem como proteínas do mosquito Anopheles . As novas proteínas analisadas foram três proteínas do Plasmodium associadas à invasão do mosquito (CTRP, TRAP e Enolase), além de uma proteína anofélica envolvida na resposta imune do mosquito contra a invasão do Plasmodium (ICHIT). Estimamos frequências características de RRM para grupos de proteínas envolvidas no ciclo de vida do Plasmodium . Posteriormente, foram estimadas as frequências eletromagnéticas esperadas, assumindo diversos cenários plausíveis para mecanismos de movimentação de carga. Com base nos resultados obtidos, propomos que a radiação eletromagnética nessas frequências será capaz de interferir nas correspondentes interações macromoleculares.
Métodos
Modelo de reconhecimento ressonante
O RRM postula que as interações proteína/DNA/RNA implicam um mecanismo de transferência de energia ressonante entre as moléculas envolvidas na frequência específica para cada função/interação observada [ 9–11 ]. O RRM descreve o cenário teórico mais provável para o reconhecimento e interação de proteínas, conseguindo superar algumas desvantagens das abordagens tradicionais baseadas na complementaridade estrutural. Ao mesmo tempo, o RRM inclui um algoritmo prático para detectar as frequências de ressonância em um grupo de proteínas análogas/ortólogas. Para isso, a estrutura primária de uma proteína é representada como uma distribuição de energias de elétrons livres ao longo da sequência, com cada aminoácido da sequência simbolizado pelo parâmetro físico-químico correspondente que descreve as energias dos elétrons livres [9–11 ] .
A série numérica resultante representa a distribuição das energias dos elétrons livres ao longo da molécula de proteína. Tais séries numéricas são então analisadas com métodos de análise de sinais digitais, utilizando a Transformada de Fourier, a fim de extrair informações pertinentes à função biológica. Como a distância entre os resíduos de aminoácidos em uma cadeia polipeptídica é de 3,8 Å, pode-se presumir que os pontos na sequência numérica são equidistantes. Para análises numéricas adicionais, a distância entre os pontos nessas sequências numéricas é definida em um valor arbitrário de d = 1. Portanto, a frequência máxima no espectro é F = 1/2d = 0,5. O número total de pontos na sequência influencia apenas a resolução do espectro. Portanto, para uma sequência de N pontos a resolução no espectro é igual a 1/N. O n-ésimo ponto da função espectral corresponde à frequência f = n/N.
Para extrair características espectrais comuns de sequências com função biológica igual ou semelhante, é utilizada a função espectral cruzada múltipla. Comparando os espectros de Fourier dessas distribuições de energia usando múltiplas funções espectrais cruzadas (espectro de consenso), descobriu-se que proteínas que compartilham a mesma função biológica compartilham a mesma periodicidade (frequência) dentro das distribuições de energia ao longo da proteína. Esta frequência comum é proposta como sendo uma frequência característica para a função biológica analisada. Além disso, descobriu-se que macromoléculas em interação (proteína/DNA/RNA) compartilham a mesma frequência, mas exibem fase oposta nesta frequência [ 9–11 , 17 ] . Assim, foi proposto que as frequências RRM caracterizam não apenas uma função geral, mas também a interação entre a proteína específica e o seu alvo, o que pode então ser considerado um reconhecimento ressonante.
Concebendo as interações macromoleculares como transferência de energia ressonante entre as moléculas em interação, a transferência de energia pode ser prevista como através de oscilações de um campo físico, possivelmente de natureza eletromagnética. Uma vez que há evidências de que as proteínas e o DNA/RNA têm certas propriedades condutoras ou semicondutoras, a carga que se move através da estrutura macromolecular e passa por diferentes estágios de energia causados pela distribuição de energias de elétrons livres ao longo da sequência da proteína pode produzir condições suficientes para um efeito eletromagnético específico. radiação ou absorção. A faixa de frequência deste campo depende da velocidade da carga. Inicialmente, o RRM propõe que a carga viaja através da estrutura macromolecular na forma de elétrons no estado sólido a uma velocidade estimada de 7,87×10 5 m / s [ 9–11 ]. Para esta velocidade e a distância entre os aminoácidos em uma molécula de proteína, que é de 3,8 Å, a faixa de frequência para interações proteicas foi estimada entre 10 12 Hz e 10 15 Hz (cenário de Cosic). Descobriu – se que essas previsões computacionais estão relacionadas à função biológica das macromoléculas por comparação com uma série de medições experimentais [ 9 , 10 ] , bem como por endosso experimental direto [ 13–16 , 18 ].
Com este cenário, propõe-se que a transferência de carga viaje através da estrutura da proteína. No entanto, se levarmos em conta a possibilidade de transferência de carga através de estruturas complexas de proteínas e, em particular, hélices alfa, poderia ser na forma de sólitons [19 ] (Davydov [ 20 , 21 ], Hyman [ 22 ], Sinkala [ 23 ]) , excitons (Davydov [ 20 , 21 ], Sinkala [ 23 ], Yomosa [ 24 ], Pang [ 25 ]) e fônons (Yomosa [ 24 ], Pang [ 25 ], Ichinose [ 26 ]). Essas outras formas de transferência de carga ocorrem em velocidades diferentes, variando de 10 5 m/s para sólitons e alguns excitons até a velocidade do som e pequenas frações da velocidade do som para fônons. Assim, com as mesmas periodicidades dentro das sequências de proteínas, conforme determinado pelo RRM, diferentes modalidades de transferência de carga podem produzir diferentes frequências de ressonância, que não estão necessariamente relacionadas à sua função biológica proteica, mas podem estar relacionadas às ressonâncias da proteína e do DNA/RNA. , em geral. Essa abordagem foi testada com tubulina e microtúbulos [ 27 ] e os resultados foram comprovados experimentalmente [ 18 ]. Além disso, aplicamos essa abordagem à telomerase como exemplo de proteínas, aos telômeros como exemplo de sequências de DNA, bem como ao mRNA de TERT como exemplo de macromoléculas de RNA [28 ] .
Sequências
Centramos nosso estudo usando análise RRM em:
- proteínas envolvidas na infecção parasitária de glóbulos vermelhos/hepatócitos,
- proteínas envolvidas no estágio Anopheline do ciclo de vida do Plasmodium ,
- proteínas propostas como candidatas a vacinas,
- alvos de eritrócitos humanos da invasão do Plasmodium ,
- proteínas envolvidas na fase do mosquito do ciclo de vida do Plasmodium .
Para obter uma lista completa das oitenta e uma sequências analisadas (alocadas em dez grupos de proteínas), consulte Arquivo adicional 1 . Os seguintes grupos foram incluídos na pesquisa atual:
Proteína de ligação à quitina intestinal (ICHIT)
O ICHIT é uma galectina com dois supostos domínios de ligação à quitina separados por uma região de mucina rica em politreonina. Os domínios de mucina do ICHIT participam na formação da matriz extracelular e na captura de patógenos microbianos. O ICHIT é considerado um marcador da resposta imune do mosquito e também é o nome do gene codificador dessa proteína, que é considerado pertencente à família de genes ‘Receptor de Reconhecimento de Padrões’ [1 ] . Oito sequências ICHIT foram analisadas.
Proteína relacionada ao circunsporozoíto e TRAP (CTRP)
A CTRP é a primeira molécula considerada essencial para a infectividade do oocineto e, consequentemente, para a transmissão da malária por mosquitos. É produzida no estágio invasivo do mosquito, ou oocineto, e é uma proteína candidata para um papel na adesão do oocineto e na invasão do epitélio do intestino médio do mosquito e é considerada uma vacina candidata para bloquear a transmissão. O CTRP contém dois tipos de domínios adesivos (relacionado ao fator de von Willebrand tipo A e relacionado à trombospondina tipo 1) e foi detectado no local de contato com a lâmina basal, sugerindo que a junção assim formada pode induzir o oocineto a se transformar em um oocisto, que foi apoiado pela interrupção direcionada de experimentos de CTRP in vivo. O CTRP também está envolvido na locomoção do oocineto no intestino médio de Anopheles e demonstrou se ligar à laminina e ao colágeno IV, principais componentes da lâmina basal, levando a sugestões adicionais de um suposto papel na transformação do oocineto em oocisto. Verificou-se que a imunidade humoral induzida naturalmente contra CTRP leva à interrupção da transmissão [ 3 ]. Seis sequências de CTRP foram analisadas.
Proteína Anônima Relacionada à Trombospondina (TRAP)
A TRAP é uma proteína expressa em esporozoítos. Durante a invasão dos anopheles, o TRAP é um ator central no deslizamento dos esporozoítos, na invasão celular e na infectividade in vivo. Verificou-se que os esporozoítos portadores de um domínio TRAP A mutado são prejudicados na invasão das glândulas salivares, mas não na motilidade de deslizamento, sugerindo que os dois processos são funcionalmente distintos e que o domínio A está envolvido no reconhecimento e/ou ligação à saliva. moléculas receptoras da glândula. A TRAP é uma das poucas vacinas candidatas propostas até agora para P. vivax. Plasmodium falciparum TRAP contribui para o desenvolvimento de proteção contra a malária grave, sugerindo que esta molécula poderia aumentar a eficiência protetora das vacinas disponíveis contra esporozoítos contra a malária [ 2 ]. Sete sequências TRAP foram analisadas.
Enolase
A Enolase de Plasmodium é uma enzima essencial na via glicolítica que catalisa a conversão de 2-fosfoglicerato em fosfoenolpiruvato. As enzimas glicolíticas parecem ser candidatas promissoras nesta perspectiva, uma vez que a produção de energia em P. falciparum depende inteiramente da via glicolítica, uma vez que o parasita e o seu hospedeiro mamífero (eritrócitos) carecem de um ciclo de Krebs completo e de mitocôndrias activas. Curiosamente, a Enolase também desempenha uma função separada: é exportada para a superfície celular dos merozoítos através de um mecanismo pouco compreendido. No Plasmodium , a Enolase de superfície auxilia na invasão das células hospedeiras ligando-se ao plasminogênio, um precursor da protease plasmática. É um alvo importante na resposta imune do mosquito, devido à sua natureza como ligante de superfície do oocineto. Aparentemente interage com células epiteliais do intestino médio. A Enolase tem sido considerada uma vacina candidata promissora [ 5 , 29 ]. Sete sequências de Enolase foram analisadas.
Proteína Circunsporozoíta (CS)
O CS desempenha um papel fundamental na invasão de hepatócitos por esporozoítos de Plasmodium . Este processo prossegue aparentemente através da interação do CS com proteoglicanos na superfície dos hepatócitos. A única vacina de fase 3 para a malária até agora é baseada na CS [ 4 , 30 ]. Dezoito sequências CS foram analisadas.
Antígeno 1 da Membrana Apical (AMA-1)
A proteína AMA-1 está envolvida na reorientação dos merozoítos, na formação de junções móveis e na vedação do vacúolo parasitóforo durante a invasão eritrocitária. Também é expresso durante os estágios esporozoíto e hepático. O AMA-1 também foi reivindicado como alvo para invasão de hepatócitos por esporozoítos, sugerindo que poderia ser considerado um candidato potencial para uma vacina multiestágio contra a malária, visando os estágios eritrocíticos e pré-eritrocíticos do hospedeiro humano [ 31 , 32 ] . Seis sequências AMA-1 foram analisadas.
Antígeno de ligação a eritrócitos (EBA175)
A proteína EBA175 é um antígeno de estágio sanguíneo que auxilia na ligação do merozoíta aos eritrócitos hospedeiros. O EBA175 é considerado uma adesina que se liga ao ácido siálico e à glicoforina A durante a invasão dos eritrócitos. O EBA175 também se liga à proteína RBC Band3, participando assim em pelo menos dois mecanismos principais de invasão de eritrócitos. Anticorpos direcionados ao EBA175 inibem a infecção de hemácias por Plasmodium . O EBA175 foi considerado uma vacina candidata promissora [ 33 ]. Oito sequências EBA175 foram analisadas.
Proteína de membrana eritrocitária de Plasmodium falciparum (PfEMP1)
O PfEMP1 foi descrito como o ligante rosetting do Plasmodium . Rosetting é o termo usado para descrever a adesão de eritrócitos infectados com eritrócitos não infectados na vasculatura do órgão infectado e está associado à malária grave. Descobriu-se que as proteínas PfEMP1 se ligam a uma ampla gama de receptores endoteliais, como CD36, molécula de adesão intercelular 1 (ICAM-1), sulfato de condroitina A, molécula de adesão de células endoteliais plaquetárias, molécula de adesão de células vasculares, ácido hialurônico, sulfato de heparam, e outras moléculas, como receptor de complemento 1, imunoglobulinas G e antígenos do grupo sanguíneo ABO. O PfEMP1 foi considerado um candidato a vacina [ 6 ]. Treze sequências de PfEMP1 foram analisadas.
Protease de Peptídeo Sinal (PfSPP)
O PfSPP se liga às proteínas Band3 da membrana das hemácias. Tem sido considerado um alvo potencial para o desenvolvimento de medicamentos antimaláricos. Quatro sequências PfSPP foram analisadas.
Proteína RBC Band3
Para estudar possíveis interações, a proteína RBC Band3 também foi analisada. A proteína Band3 é uma proteína de transporte de membrana onipresente encontrada na membrana plasmática de diversos tipos de células e tecidos. É a principal proteína transmembrana integral da membrana plasmática dos eritrócitos, compreendendo 25% da proteína total da membrana. Permite a troca de bicarbonato/cloreto através das membranas celulares dos eritrócitos, bem como o influxo de lactato para os glóbulos vermelhos. Foi levantada a hipótese de que a principal via de invasão de hemácias pelos merozoítos ocorre através de uma via dependente de Band3. A presença de proteína semelhante a Band3 em hepatócitos também foi sugerida [ 7 ]. Quatro sequências de RBC Band3 foram analisadas.
Resultados e discussão
Aqui, utilizamos o modelo RRM para analisar as proteínas envolvidas no ciclo de vida do Plasmodium , incluindo a interação com o hospedeiro humano. O objetivo era descobrir frequências características para esses grupos funcionais de proteínas e para suas interações. Posteriormente, objetivou-se identificar frequências eletromagnéticas relacionadas a essas frequências características e funções/interações relacionadas. Se identificarmos uma frequência que é vital para a interação do Plasmodium com o hospedeiro, existe a possibilidade de interferir nessa frequência e prevenir a interação com o hospedeiro (infecção).
Analisámos todos os grupos listados de proteínas relacionadas com a malária e obtivemos os seguintes resultados:
Proteínas de Anopheles envolvidas na invasão do Plasmodium
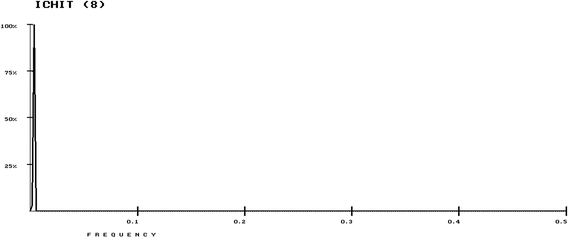
O espectro de consenso para ICHIT mostra um único pico comum proeminente na frequência de f = 0,0034, conforme apresentado na Fig .
Espectro de consenso para oito proteínas ICHIT com pico comum único proeminente na frequência de f = 0,0034
Proteínas de Plasmodium envolvidas na invasão de anopheles
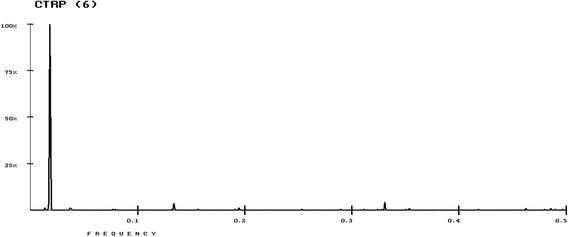
A partir do espectro de consenso para CTRP, conforme apresentado na Fig. 2 , podem ser observados vários picos, talvez reflectindo as múltiplas funções atribuídas a esta proteína. Como é aparente, o pico principal aparece na frequência de f = 0,0186. Outros picos aparecem na frequência de f = 0,0034, na frequência de f = 0,11 e na frequência de f = 0,34.
Espectro de consenso para seis proteínas CTRP, o pico principal aparece na frequência de f = 0,0186. Outros picos aparecem na frequência de f = 0,0034, na frequência de f = 0,11 e na frequência de f = 0,34
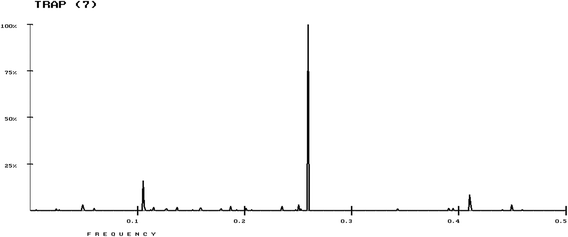
O espectro de consenso para TRAP é apresentado na Fig . O pico principal aparece na frequência de f = 0,2508, enquanto um segundo pico aparece na frequência de f = 0,11.
Espectro de consenso para sete proteínas TRAP, o pico principal aparece na frequência de f = 0,3496, enquanto outro pico aparece na frequência de f = 0,43
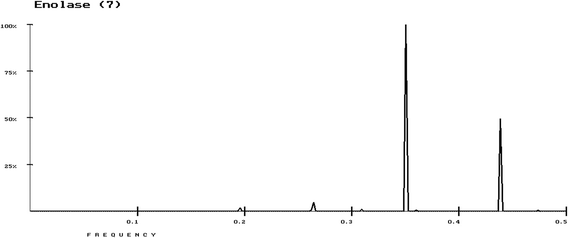
O espectro de consenso para Enolase é apresentado na Fig . O pico principal aparece na frequência de f = 0,3496, enquanto outro pico aparece na frequência de f = 0,43.
Espectro de consenso para sete proteínas Enolase, o pico principal aparece na frequência de f = 0,3496, enquanto outro pico aparece na frequência de f = 0,43
Proteínas de Plasmodium envolvidas na invasão do hospedeiro humano
Os espectros de consenso para proteínas do Plasmodium envolvidas na interação com o hospedeiro humano foram discutidos em detalhes em nosso artigo anterior [ 17 ]. Aqui descrevemos os aspectos mais salientes desse estudo.
Quando o RRM foi aplicado a dezoito proteínas CS, apenas um pico proeminente apareceu na frequência de f = 0,002. Esta frequência é compartilhada também pelas proteínas EBA175, bem como pelas proteínas PfEMP1. CS de espécies de Plasmodium com estágios dormentes ( P. cynomolgi e P. vivax ) exibiram um pico adicional na frequência de f = 0,334. Porém, CS de P. falciparum apresentou apenas o pico comum na frequência de f = 0,002.
Em resumo, para proteínas de Plasmodium interagindo com o hospedeiro humano, as frequências dos principais picos são apresentadas na Tabela 1 .
Proteínas humanas interagindo com proteínas do plasmódio
As proteínas RBC Band3 dos glóbulos vermelhos compartilham a mesma frequência de f = 0,11 com EBA175, mas com fase oposta nessa frequência, confirmando assim a interação conhecida entre essas duas proteínas durante a invasão eritrocitária [17 ] .
Estimativa de comprimentos de onda eletromagnéticos de acordo com diferentes mecanismos de transferência de carga
O RRM propõe que a interação entre macromoléculas, incluindo proteínas, seja baseada na transferência de energia eletromagnética ressonante. A frequência desta energia eletromagnética dependerá da periodicidade da distribuição de energia dos elétrons livres ao longo da proteína, conforme calculado pelo RRM, bem como da velocidade com que as cargas estão viajando. Como foram propostos diferentes mecanismos de transferência de carga, mais de uma frequência estará associada a uma única frequência RRM.
Diferentes frequências foram identificadas, mas as três seguintes frequências foram encontradas no número de diferentes grupos de proteínas e, portanto, são de especial interesse: frequência de f = 0,002, frequência de f = 0,11 e frequência de f = 0,34. Essas três frequências podem ser consideradas características da vitalidade do parasita em geral. Assim, propomos que a vitalidade do parasita pode ser diminuída pela interferência em algumas dessas três frequências RRM. Para descobrir as frequências eletromagnéticas correspondentes, introduzimos as diferentes modalidades de transferência de carga, conforme descrito acima. As frequências eletromagnéticas correspondentes dependendo das diferentes velocidades de carga são apresentadas na Tabela 2 . Estes resultados mostraram que possíveis frequências ressonantes relevantes para a vitalidade do parasita podem estar dentro de diferentes faixas de frequência (THz, GHz, MHz e até KHz), dependendo do mecanismo e da velocidade de carga dentro da estrutura da proteína.
Por outro lado, a frequência na faixa de f = 0,002-0,0078 dentro do erro de cálculo aparece como um pico muito proeminente em quatro dos dez grupos de proteínas estudados, incluindo ICHIT, CS, EBA175 e PfEMP1. Os papéis desempenhados por estas proteínas são muito diversos, no entanto os nossos resultados mostram que existe uma frequência característica comum para todas estas proteínas analisadas e assim propomos que a frequência de f = 0,002 é um papel fundamental para a vitalidade do Plasmodium . Além disso, também reduzimos a velocidade de carga, conforme proposto pelo cenário de Cosic, que no passado se mostrou relevante para a função biológica das proteínas [ 27 , 28 ]. Assim, propomos aqui que a frequência mais provável a ser utilizada para interferir na atividade do parasita é a frequência de 2-5THz.
Com estes resultados em mente, é possível considerar que em vez de várias centenas de proteínas, o mecanismo de invasão celular pode ser avaliado através de um número consideravelmente menor de frequências eletromagnéticas. Assim, a teoria do MRR propõe uma forma alternativa mais simples de lidar com o problema da invasão da malária.
Conclusão
Nossos resultados revelaram que, apesar da diversidade estrutural e funcional, bem como das diferenças em sua origem, dez grupos de proteínas estudados compartilharam pelo menos uma das três frequências RRM a seguir (f = 0,002, f = 0,11 ou f = 0,34). Particularmente onipresente foi a frequência de f = 0,002 (0,002-0,0078), que apareceu como o pico principal dos espectros de consenso para proteínas que desempenham papéis tão diversos como imunidade ao receptor de reconhecimento de padrões em mosquitos, invasão de hepatócitos, anticorpos para proteínas humanas e formação de rosetas de eritrócitos. Assim, a frequência de f = 0,002 foi proposta como a principal frequência RRM envolvida na vitalidade do Plasmodium . Isto provavelmente corresponderia a uma frequência infravermelha de 2-5THz. Assim, interferir nesta frequência a partir de uma fonte infravermelha deverá interromper o processo de invasão da malária. Embora esta frequência eletromagnética infravermelha distante não possa penetrar no corpo humano mais do que 4 cm [ 34 ], tal radiação pode ser de grande ajuda no combate ao Plasmodium , uma vez que uma parte considerável do parasita permanece na pele por horas após a picada do mosquito. Além disso, a frequência RRM específica é capaz de iniciar de forma ressonante toda uma cascata de interações proteína-proteína (DNA, RNA) direcionadas à atividade biológica específica que poderia neutralizar a infecção por Plasmodium .
Abreviações
- AMA-1:
- Antígeno de Membrana Apical 1
- CS:
- Proteína Circunsporozoíta
- CTRP:
- Proteína relacionada ao circunsporozoíto e TRAP
- ADN:
- Ácido desoxirribonucleico
- EBA175:
- Antígeno de ligação a eritrócitos 175
- ICHIT:
- Proteína de ligação à quitina intestinal
- PfEMP1:
- Proteína 1 da membrana eritrocitária de Plasmodium falciparum
- PfSPP:
- Protease de peptídeo sinal de Plasmodium falciparum
- RBC:
- Glóbulos vermelhos
- ARN:
- Ácido ribonucleico
- RRM:
- Modelo de reconhecimento ressonante
- TERCEIRO:
- Transcriptase reversa da telomerase
- ARMADILHA:
- Proteína Anônima Relacionada à Trombospondina
Referências
-
Tahar R, Boudin C, Thiery I, Bourgouin C. Resposta imunológica de Anopheles gambiae aos estágios esporogônicos iniciais do parasita da malária humana Plasmodium falciparum. EMBO J. 2002;21:6673–80.
-
Sultan AA, Thathy V, Frevert U, Robson K, Crisanti A, Nussenzweig V, et al. TRAP é necessário para o deslizamento da motilidade e infectividade dos esporozoítos do plasmódio. Célula. 1997;90:511–22.
-
Kaneko O, Templeton TJ, Iriko H, Tachibana M, Otsuki H, Takeo S, et al. O Plasmodium vivax homólogo da proteína micronemal adesiva do oocineto. CTRP Parasitol Int. 2006;55:227–31.
-
Ying P, Shakibaei M, Patankar MS, Clavijo P, Beavis RC, Frevert U. A proteína circunsporozoíta da malária: interação das regiões conservadas i e ii-plus com oligossacarídeos semelhantes à heparina em sulfato de heparano. Exp Parasitol. 1997;85:168–82.
-
Pal-Bhowmick I, Mehta M, Coppens I, Sharma S, Jarori GK. Propriedades protetoras e localização superficial da enolase de Plasmodium falciparum. Infectar imunidade. 2007;75:5500–8.
-
Chen Q, Barragan A, Fernandez V, Sundström A, Schlichtherle M, Sahlén A, et al. Identificação da proteína 1 da membrana eritrocitária do Plasmodium falciparum (PfEMP1) como o ligante rosetting do parasita da malária P. falciparum. J Exp Med. 1998;187:15–23.
-
Goel VK, Li X, Chen H, Liu SC, Chishti AH, Oh SS. A banda 3 é um receptor hospedeiro que se liga à proteína 1 da superfície do merozoíto durante a invasão dos eritrócitos pelo Plasmodium falciparum. Proc Natl Acad Sci US A. 2003;100:5164–9.
-
Wilbanks AD. Sistema infravermelho para matar insetos/mosquitos. Patente dos EUA, US6050025 A. US 08/761.282; 2000.
-
Cosic I. Bioatividade Macromolecular: É Interação Ressonante entre Macromoléculas?-Teoria e Aplicações. IEEE Trans em Engenharia Biomédica. 1994;41:1101–14.
-
Cosic I. O Modelo de Reconhecimento Ressonante da Bioatividade Macromolecular: Teoria e Aplicações. Basileia: Birkhauser Verlag; 1997.
-
Cosic I, Nesic D. Predição de ‘pontos quentes’ no intensificador SV40 e relação com dados experimentais. Eur J Biochem. 1988;170:247–52.
-
Istivan T, Pirogova E, Gan E, Almansour NM, Coloe PJ, Cosic I. Efeitos biológicos de um análogo peptídico do vírus mixoma projetado de novo: Avaliação da citotoxicidade em células tumorais. PLoS UM. 2011;6(9), e24809.
-
Vojisavljevic V, Pirogova E, Cosic I. O efeito da radiação eletromagnética (550 nm-850nm) na cinética da I-lactato desidrogenase. Internat J Radiat Biol. 2007;83:221–30.
-
Wu HPP, Persinger MA. Aumento da mobilidade e taxa de proliferação de células-tronco em Dugesia tigrina induzida por diodo emissor de luz de 880 nm. J Photochem Photobiol B Biol. 2011;102:156–60.
-
Murugan NJ, Karbowski LM, Persinger MA. O modelo de reconhecimento de ressonância de Cosic para sequências de proteínas e emissão de fótons diferencia cepas letais e não letais de Ebola: implicações para o tratamento. Abra J Biofísica. 2014;5:35.
-
Dotta BT, Murugan NJ, Karbowski LM, Lafrenie RM, Persinger MA. Mudança de comprimento de onda das emissões de fótons ultrafracos de células de melanoma moribundas: seu aprimoramento e bloqueio químico são previstos pela teoria do modelo de reconhecimento ressonante de Cosic para macromoléculas. Naturwissenschaften. 2014, 101(2); doi: 10.1007/s00114-013-1133-3 .
-
Cáceres JLH, Cosic D, Cosic I. Aplicação do modelo de reconhecimento ressonante ao estudo das proteínas do plasmódio envolvidas na infecção da malária. Dados Médicos MD. 2015;7:7–14.
-
Sahu S, Ghosh S, Fujita D, Bandyopadhyay A. Visualizações ao vivo da automontagem de proteína tubulina isolada única via corrente de tunelamento: efeito do bombeamento eletromagnético durante o crescimento espontâneo de microtúbulos. Relatórios Científicos. 2014;4 . doi:10.1038/srep07303.
-
Ciblis P, Cosic I. A Possibilidade de Transferência Soliton/Exciton em Proteínas. J Theor Biol. 1997;184:331–8.
-
Davidov AS. Excitons e Sólitons em Sistemas Moleculares. Int Rev Cytol. 1987;106:183–225.
-
Davidov AS. Influência da interação elétron-fônon no movimento de um elétron em um sistema molecular unidimensional. Teoreticheskaya e Matematicheskaya Fizika. 1979;40:408–21.
-
Hyman JM, McLaughlin DW, Scott AC. Nos Sólitons Alpha-Helix de Davydov, Predição de Longo Tempo em Dinâmica. John Wiley & Sons, INC, NY; 1983. pág. 367–394.
-
Sinkala Z. Transporte Soliton/Exciton em Proteínas. J Theor Biol. 2006;241:919–27.
-
Yomosa S. O Exciton em Proteína. J Física Soc Japão. 1963;18(10):1494.
-
Pang XF. Teoria do Transporte de Bioenergia em Moléculas de Proteínas e suas Evidências Experimentais, bem como Aplicações. Frente. Física. China 2007; 2(4):469-93.
-
Excitações de Ichinose S. Soliton em estruturas de proteínas alfa-helicoidais. Caos, Fractais Solitons. 1991;1:501–9.
-
Cosic I, Lazar K, Cosic D. Predição de frequências ressonantes de tubulina usando o modelo de reconhecimento ressonante (RRM). IEEE Trans em NanoBiociência. 2015;12:491–6. doi: 10.1109/TNB.2014.2365851 .
-
Cosic I, Cosic D, Lazar K. É possível prever ressonâncias eletromagnéticas em proteínas, DNA e RNA?. Física Biomédica Não Linear. 2015;3. doi:10.1140/s40366-015-0020-6.
-
Ghosh AK, Jacobs-Lorena M. Enolases de Plasmodium expressas na superfície e outros patógenos. Mem. Inst. Osvaldo Cruz. 2011, 106(1); doi: 10.1590/S0074-02762011000900011 .
-
Stewart VA, McGrath SM, Dubois PM, Pau MG, Mettens P, Shott J, et al. A preparação com uma vacina de proteína 35-circunsporozoíta (CS) de adenovírus seguida de RTS, o reforço de S/AS01B melhora significativamente a imunogenicidade para Plasmodium falciparum CS em comparação com qualquer uma das vacinas contra a malária isoladamente. Infectar imunidade. 2007;75:2283–90.
-
Yandar N, Pastorin G, Prato M, Bianco A, Patarroyo ME, Lozano JM. Perfil imunológico do conjugado peptídeo N-terminal-nanotubo de carbono de Plasmodium vivax AMA-1 em um modelo de camundongo infectado por Plasmodium berghei. Vacina. 2008;26:5864–73.
-
Silvie O, Franetich JF, Charrin S, Mueller MS, Siau A, Bodescot M, et al. Um papel para o antígeno 1 da membrana apical durante a invasão de hepatócitos por porozoítos de Plasmodium falciparum. J Biol Química. 2004;279:9490–6.
-
Tolia NH, Enemark E, Sim BK, Joshua-Tor L. Base estrutural para a via de invasão de eritrócitos EBA-175 do parasita da malária Plasmodium falciparum. Célula. 2005;122:183–93.
-
Vatansever F, Hamblin MR. Radiação infravermelha distante (FIR): seus efeitos biológicos e aplicações médicas. Lasers Fotônicos Med. 2012;1(4):255–66. doi: 10.1515/plm-2012-0034 .
Agradecimentos
O atual trabalho de pesquisa é financiado pela AMALNA Consulting, empresa registrada de consultoria e pesquisa, Austrália.
Informação sobre o autor
Autores e Afiliações
-
Universidade RMIT, Melbourne, VIC, Austrália
Irena Cosic
-
AMALNA Consulting, Black Rock, VIC, Austrália
Irena Cosic e Drasko Cosic
-
Escola de Medicina e Ciências Aliadas da Saúde, Universidade da Gâmbia, Sere Kunda, Gâmbia
José Luís Hernandes Cáceres
autor correspondente
Correspondência para Irena Cosic .
Informações adicionais
Interesses competitivos
Os autores declaram não ter interesses conflitantes.
Contribuições dos autores
IC introduziu a ideia de frequências RRM e radiação eletromagnética e escreveu uma parte e supervisionou todo o artigo. JLHC conceituou e escreveu parte do artigo. DC realizou os cálculos e analisou os resultados. Todos os autores leram e aprovaram o manuscrito final.
Arquivo adicional
Arquivo adicional 1:
Sequências submetidas à análise RRM. (DOCX 17kb)
Direitos e permissões
Acesso aberto Este artigo é distribuído sob os termos da Licença Internacional Creative Commons Atribuição 4.0 ( http://creativecommons.org/licenses/by/4.0/ ), que permite uso, distribuição e reprodução irrestrita em qualquer meio, desde que você forneça crédito apropriado ao(s) autor(es) original(is) e à fonte, forneça um link para a licença Creative Commons e indique se alterações foram feitas.
Fonte: https://epjnonlinearbiomedphys.springeropen.com/articles/10.1140/epjnbp/s40366-015-0025-1